السّماد واسع الانتشار الّذي يستخدمه المجرمون كموادّ متفجّرة: ما حقيقة المادّة الّتي أدّت، على ما يبدو، للانفجار المُدمّر والقاتل في مرفأ بيروت؟
لقيَ أكثر من مئة شخص حتفهم، وأصيب المئات، ولحقت أضرار هائلة بمناطق شاسعة من المدينة، في الانفجار الضخم الّذي حدث في هذا الشهر في ميناء بيروت. تشير التّقارير الأوّليّة إلى أنَّ مادة نيترات الأمونيوم كانت هي المسبّب للانفجار، حيث تُستخدَم هذه المادّة كسمادٍ زراعيّ واسع الانتشار، وقد أدّت في الماضي إلى سلسلة من الكوارث الصّعبة. نيترات الأمونيوم هو مُركَّب نيتروجينيّ، ويعتبر النّيتروجين إحدى المواد المركزيّة في استمراريّة الحياة على الكرة الأرضيّة ودوامها، وهو مُكوّنٌ أساسيّ في الصّناعات الحديثة أيضًا.
سمادٌ من الهواء
النّيتروجين هو العنصر الأكثر انتشارًا في الغلاف الجوّيّ للكرة الأرضيّة- يٌشكّل النّيتروجين الصافي حوالي 80 بالمئة من الهواء الّذي نتنفّسه. والنّيتروجين هو مادة من الموادّ الأكثر ضروريّة للحياة: فهو حجر الأساس في بناء البروتينات (الأحماض الأمينيّة)، ويدخل كذلك ، في تركيب جزيئات الـ DNA والـ RNA وموادّ أخرى تشارك في مختلف العمليّات البيولوجيّة الضّروريّة. والأمر المفاجئ أنّ كمّيّة النّيتروجين المتوفّرة بين أيدينا للاستخدام قليلةٌ جدًّا، بالرّغم من تواجده بوفرةٍ في الغلاف الجوّيّ. يتواجد النّيتروجين في الغلاف الجوّيّ بشكل جزيئات ثنائيّة الذّرّات، N2، تكون فيها ذرّات النّيتروجين مربوطةً فيما بينها برابط قويّ جدًّا (رابط ثلاثيّ). المخلوقات الوحيدة الّتي تستطيع تفكيك نيتروجين الغلاف الجوّيّ هي الطّحالب، وأنواعٌ معيّنةٌ من البكتيريا، خاصةً بكتيريا التّربة الّتي تُكوّن من النّيتروجين والهيدروجين مركَّب الأمونيا: NH3. تُكوّن أنواعٌ أخرى من البكتيريا أكاسيدَ نيتروجينيّة من الأمونيا، تحتوي هذه الأكاسيد على عنصري النّيتروجين والأكسجين، مثلًا النّتريت، -NO2، و النّيترات، -NO3 . تستطيع النّباتات استيعاب هذه المركبات ودمجها في الموادّ البيولوجيّة المذكورة، وتصل مركّبات النّيتروجين بهذه الطّريقة إلى آكلي النّباتات والحيوانات المفترسة، وإلى سائر الأحياء.
وتُنتَج مركّبات النّيترات أيضًا في عمليّاتٍ غير بيولوجيّة معيّنة مثل البرق، وانفجار الحمم البركانيّة، إذ تتكوّن معادن تحتوي على النّيترات، أشهرها السّالبيتر (الملح الصّخريّ)، وهو خليط من نيترات البوتاسيوم، KNO3 و نيترات الصّوديوم، NaNO3.
تكتفي النّباتات الّتي تنمو في الطّبيعة بكمّيّات النّيتروجين الّتي تحصل عليها من المعادن والبكتيريا، أمّا إذا أردنا تكثيف الزّراعة والحصول على كمّيّات كبيرة من المحصول عامًا بعد عام، فلن تكفينا كمّيّات النّيتروجين الموجودة في التّربة لهذا الغرض، ويجب تخصيب التّربة بالنّيتروجين (وعناصر أخرى) من مصادر أخرى.
كانت إفرازات (رّوْث) الحيوانات هي مصدر النّيتروجين الرّئيسيّ في الزّراعة إلى أن شرعَ العلماء بتطوير أسمدة كيميائيّة أكثر نجاعةً، أدّت هذه المشاريع إلى ازدياد هائل في طلب مرابض السّالبيتر الكبيرة في شمال تشيلي، وأدّى ذلك إلى حدوث نزاعات عسكريّة. مع بداية القرن العشرين طوّرَ العالِم الألمانيّ فريتز هابر (Haber) عمليّةً صناعيّةً لإنتاج الأمونيا من نيتروجين الجوّ. أنتجت الصّناعة الألمانيّة حمض النّيتريك (HNO3)، الّذي يُعتبَر أساس جميع النّيترات، من الأمونيا بواسطة الدّمج بين عمليّة هابر وعمليّةٍ أخرى طوّرها عالِم ألمانيّ آخر اسمه أوستوالد (Ostwald). أصبح بذلك لدى ألمانيا مصدرًا غير منقطع من السّماد الزّراعيّ، وقد أنقذها ذلك من المجاعة في الحرب العالميّة الأولى.
المورد الطبيعيّ الّذي أدّى إلى نزاعات عسكريّة. مصنع السّلابتر المتروك في شمال تشيلي | تصوير: Przemysław Skibiński, Shutterstock
نيتروجين قابل للانفجار
استخدمت ألمانيا مركّبات النّيترات لأغراض أخرى عدا عن تسميد الحقول الزّراعيّة. تنبعث كمّيّة كبيرة من الطّاقة من الأكاسيد النّيتروجينيّة عند تفكّكها، ممّا جعلها مُكوّنًا مهمًّا في الموادّ المتفجّرة. استُخدمت مثل هذه الأكاسيد كبارودٍ في الصّين القديمة، واكتُشفت في القرن التّاسع عشر أهميّتها في الموادّ المتفجّرة الأشدّ قوةً، مثل النّيتروجليسرين والدّيناميت الّذي طوّر ألفرد نوبل الـ TNT منه. تعتمد هذه الموادّ المتفجّرة على مجموعة النّيترو، NO2، ومجموعة النّيترات الّتي تتّصف بميزتين: الأولى هي ميل ذرّات النّيتروجين الّتي فيها للاتّحاد فيما بينها، وتكوين جزيئات N2 من خلال تفاعل كيميائيّ مشعّ للطّاقة، إذ تنبعث كمّيّة كبيرة من الطّاقة الحراريّة إلى البيئة المحيطة عند حصوله. أمّا الميزة الثّانية فهي انطلاق الأكسجين في هذه العمليّة، إذيعمل هذا الأكسجين على احتراق المُكوّنات الأخرى في المادّة المتفجّرة بنجاعة دون الحاجة إلى تزويد الأكسجين من الهواء. تؤدّي الحرارة والأكسجين وانبعاث كمّيّة كبيرة من الغازات خلال وقت قصير إلى ردِّ فعل شديدٍ وسريع، نراه ونشعر به على شكل انفجار.
تُستخدَم المركّبات النّيتروجينيّة في العصر الحاضر أيضًا في موادّ متفجّرة متطوّرة ومتنوّعة، بدءًا ببارود المفرقعات النّاريّة، مرورًا بالموادّ المتفجّرة البلاستيكيّة، مثل C4 أو السّمتكس (Semtex)، وانتهاءً بالموادّ الّتي تؤدّي إلى انتفاخ الوسادات الهوائيّة في السّيارات بغاز النّيتروجين.
ما زالت تُستخدم مركّبات النّيتروجين كسماد زراعيّ مهم في أيّامنا هذه. إذ تُزوّد الأمونيا واليوريا (CO(NH2)2) ونيترات البوتاسيوم النّباتات بالنّيتروجين، ولكنّ هذه المواد تُستخدم أحيانًا من قِبَل منظّمات إرهابيّة لإنتاج الموادّ المتفجّرة. نيترات الأمونيوم هي مادّة أخرى لها استخدام مزدوَج، وهي الّتي أدت على ما يبدو، وفقًا للتقارير المختلفة، إلى الانفجار الهائل في بيروت.
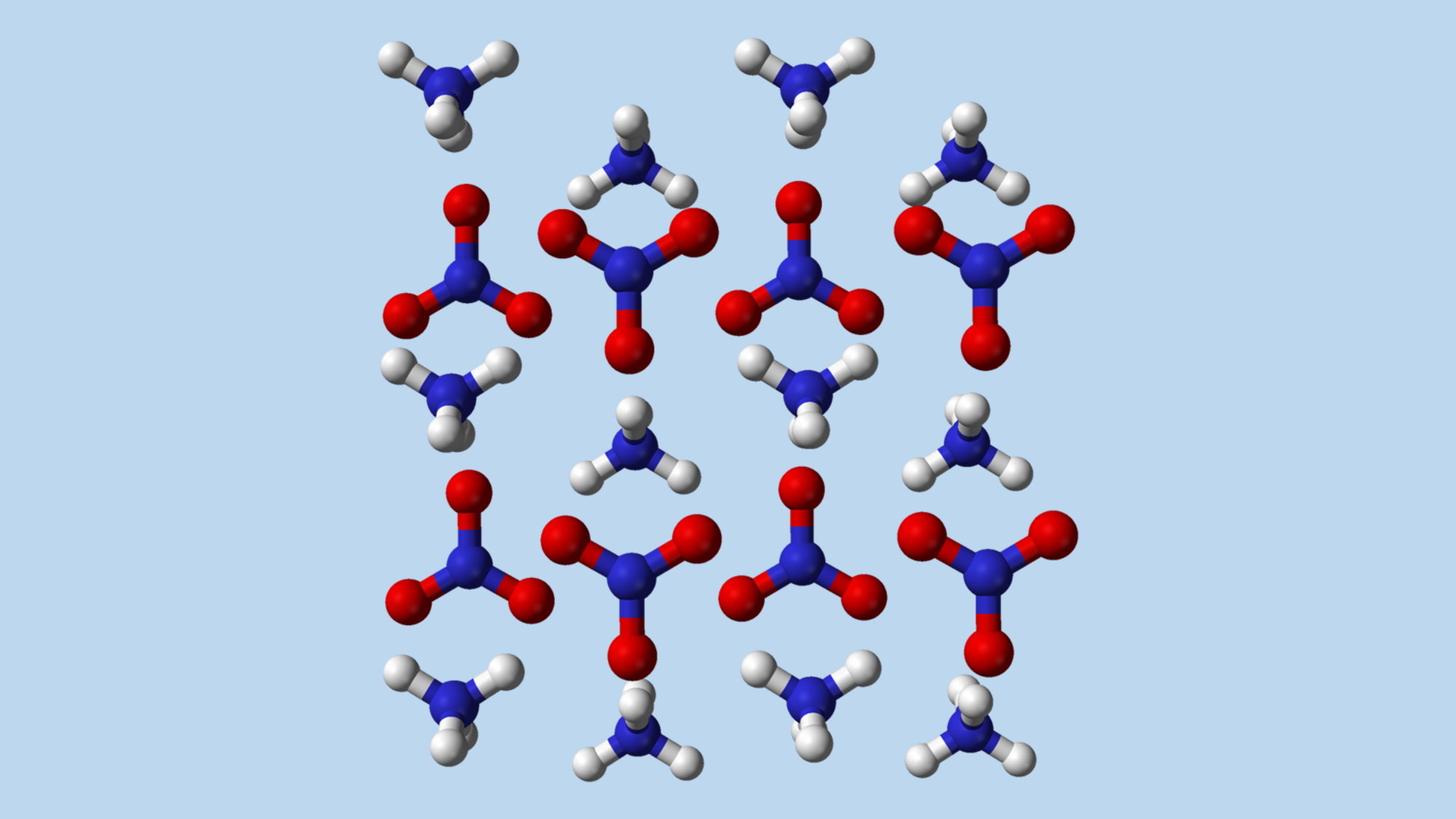
المادّة ذات الاستخدام المزدوَج. جسيمات نييترات الأمونيوم (النّيتروجين - بالأزرق، الأكسجين - بالأحمر، الهيدروجين - بالأبيض) | المصدر: ويكيبيديا, مُتاح للجميع
خاملٌ وخطير
يتكوّن مركّب نيترات الأمونيوم، كما يدلّ اسمه، من النّيترات والأمونيوم وصيغته NH4NO3. نيترات الأمونيوم هو سمادٌ شائعٌ وشعبيٌّ بفضل احتوائه على نسبة عالية من النّيتروجين، وبفضل سهولة عمليّة إنتاجه بتكلفة قليلة. يمكن إنتاج موادّ متفجّرة أخرى من نيترات الأمونيوم بفضل الصّفات ذاتها والّتي جعلته سمادًا شائعًا وشعبيًّا. مثلًا: تنتج المادّة المتفجّرة الّتي تُسمّى ANFO (اختصار الكلمات: Ammonium Nitrate Fuel Oil) من خلط نيترات الأمونيوم بنسبة 94 بالمئة مع السّولار، أو أيّ وقودٍ آخر شبيه بالسّولار. استُخدمت هذه المادّة في العديد من الهجمات "الإرهابيّة" مثل هجمات العصابات الإيرلنديّة في بريطانيا. قام إرهابيّون أمريكيّون في 19 نيسان / أبريل سنة 1995 بتفجير حوالي 2000 كغم من الـ ANFO المُحَسّن، بواسطة خلط نيترات الأمونيوم مع النّيتروميثان بدلًا من الوقود العاديّ، بجانب بناية مكاتب فدراليّة في أوكلاهوما سيتي، وكان الانفجار هائلًا، حيث أدّى إلى مقتل 168 شخصًا، وإصابة المئات، وإلحاق أضرار كبيرة بالمباني في منطقة الانفجار.
نيترات الأمونيوم هي مادّة خاملة فيما إذا خُزّنت في ظروف مؤاتية، ولكنها قد تتحوّل إلى مادّة خطيرة، حتّى دون تحويلها إلى مادّة متفجّرة، في حال تغيّرت الظّروف في محيط المكان الّذي تتواجد فيه. ينصهر نيترات الأمونيوم ويتحوّل من الحالة الصّلبة إلى الحالة السّائلة عند درجة حرارة 170 درجة مئويّة (سلزيوس)، ثمّ يتفكّك بعدها إلى أمونيا وأكاسيد نيتروجينيّة. هذه الأكاسيد تٌزوّد الأوكسجين الّذي يساعد على الاشتعال، فتشكّل بذلك مصدرًا يُغَذّي العامل الّذي أدّى إلى بداية الاحترار. يتفكّك المزيد من نيترات الأمونيوم إذا استمرّت عمليّة الاحتراق، ويتكوّن المزيد من الأكاسيد النّيتروجينيّة. تتحلّل الأمونيا أيضًا، وتنتج من تحلّلها كمّيّة كبيرة من الغازات. تتراكم الغازات النّاتجة بسرعة، وتؤدّي إلى تكوّن ضغطٍ عالٍ، عندما يحدث ذلك في فضاء مغلق، مما يؤدي إلى انفجار شديد. تزداد شدّة الانفجار الّذي قد يحدث مع ازدياد كمّيّة نيترات الأمونيوم المخزّنة في الفضاء المغلق. أشارت التّقارير الواردة من بيروت إلى أنَّ كمّيّة نيترات الأمونيوم الّتي وُجدت في المخزن الّذي انفجر كانت أكثر من 2000 طنّ.
قد تزداد حساسيّة نيترات الأمونيوم وخطر انفجاره إذا خُزِّنَ مع موادّ أخرى، مثل الوقود على أنواعه أو موادّ جافّة كنشارة الخشب، أو أسمدة أخرى تحتوي على مركّبات الفوسفور والكلور. وقد يؤدّي حدوث اشتعال بسيط لمثل هذه الموادّ إلى بداية تحلّل نيترات الأمونيوم وانبعاث الغازات، وعلى رأسها غاز الأكسجين، الذي يغذي الحريق الأوّليّ، ويعمل على زيادته بشكل تدريجيّ. وقد يؤدي نشوب حريق في مخزن مجاور إلى انبعاث حرارة تكفي لبدء عمليّة تحلّل نيترات الأمونيوم.
تُعتبر الفترة الزّمنيّة الّتي يُخزّن فيها نيترات الأمونيوم عاملًا آخر من شأنه أن يؤدّي إلى تحلّله. يُخزّن نيترات الأمونيوم غالبًا في أكياس قد تتمزّق، أو تتفكّك مع مرور الزّمن، خاصةً إذا خُزّنت في ظروف غير مؤاتية. إذ يزيد ذلك من تعرّض المادّة للظّروف المحيطة، ومن خطر تلوّثها وفقدان ثباتها. أشارت التّقارير المتعلّقة بانفجار بيروت إلى أنَّ نيترات الأمونيوم كان مخزّنًا في ظروف غير مناسبة لمدة زادت عن ستّ سنوات.

قد تصبح المادّة الخاملة خطيرة في ظروف معيّنة. حبيبات من نيترات الأمونيوم. | تصوير: Ihor Matsiievskyi, Shutterstock
سلسلة من الكوارث
كان الانفجار الّذي حدث في بيروت هو الحلقة الأخيرة، في الوقت الحاضر على الأقلّ، من سلسلة طويلة من الحوادث والكوارث الّتي نجمت عن الإهمال في التّعامل مع مادّة نيترات الأمونيوم.
وقعت إحدى الحوادث الشّهيرة في أبريل/ نيسان سنة 1947 في ميناء تكساس سيتي في الولايات المتحدة، حيث نشب حريق أثناء تحميل نيترات الأمونيوم على السّفينة، بعد أن تجمّعَ في مخازنها أكثر من 2000 طن من السّماد. أصدرَ رُبّان السّفينة أمرًا بإغلاق المخزن إغلاقًا مُحكمًا، ورش تيار قويّ من بخار الماء السّاخن داخله لإخماد النّار. كانت هذه العمليّة مُجديةً بشكل جزئيّ فقط، لأنّ تحلّل نييترات الأمونيوم، الّذي كان قد بدأ، أدّى إلى انبعاث الأكسجين الّذي زاد من الاشتعال، ولم يكن بمقدور الماء إيقاف العمليّة. انفجرت السّفينة بعد ساعة من نشوب الحريق، وأدّى انفجارها، لسوء الحظ، إلى نشوب حريق في سفينة مجاورة رست على بعد 250 مترًا من الانفجار، وتحمل مئات الأطنان من نيترات الأمونيوم والكبريت في مخازنها. حدث انفجار مزدوَج هائل أدّى إلى تهشيم الزّجاج على بعد 60 كيلومترًا من الميناء، ولاقى 580 شخصًا حتفَهم، وأصيب الآلاف نتيجة للانفجار.
لقي 561 شخصًا حتفهم سنة 1921 في أوباو، ألمانيا، نتيجة انفجار حدث في مصنع للأسمدة، نجم عن اشتعال نيترات الأمونيوم وكبريتات الأمونيوم، بعد أن تصلّبت هذه المواد، وأصبحت كتلة واحدة متماسكة، وحاولوا تفكيكها بواسطة موادّ متفجرة. وقُتل 189 شخصًا سنة 1942 في انفجار حدث في بلجيكا، عندما جرت محاولة لتفكيك مجمَّع كبير من نيترات الأمونيوم، الّتي تصلّبت وتكتّلت، بطريقة مشابهة. وقعت كذلك حوادث وكوارث كثيرة أخرى بأعداد أقلّ من المصابين. وبذلك يكون قد لاقى أكثر من 1000 شخص حتفهم خلال القرن العشرين في حوادث نيترات الأمونيوم.
لم تتوقف الحوادث في القرن الحادي والعشرين، إذ قُتلَ 15 شخصًا سنة 2013 في حريق اندلع في مخزن نيترات الأمونيوم في تكساس، ولاقى 173 شخصًا مصرعهم قبل خمس سنوات في انفجار مخزن نيترات الأمونيوم في ميناء تيانجين في الصّين، حدث هذا الانفجار بسبب حريق اشتعل في مخزن مجاور.

أحد أقوى الانفجارات غير النّووية في التّاريخ. موقف سيّارات يبعد 400 متر عن ميناء تكساس سيتي بعد حدوث الانفجار في الميناء. | المصدر: University of Houston Digital Library, متاح للجميع
احتراق غير تامّ
تشير التّقارير الواردة حتّى الآن إلى أنّ الانفجار في بيروت نجم هو الآخر عن حريق، إلّا أنّه لم يتّضح بعد فيما إذا كانت النّار قد اندلعت في مخزن نيترات الأمونيوم أو أنّ الاشتعال بدأ في مكان مجاور. لا يوجد حاليًّا تأكيد من الجهات الرّسميّة بأنَّ الانفجار قد نجم عن نيترات الأمونيوم. أشارت التّقارير الأوّليّة إلى أنّ نشوب حريق في مخزن مجاور للمفرقعات النّاريّة أدّى إلى اندلاع النّار الّتي أدّت بدورها إلى انفجار السّماد. يُحتمل أنَّ وجود موادّ أخرى أدّى إلى تعاظم خطر حدوث الانفجار.
تُنتَج من التّحلل التّامّ لنيترات الأمونيوم غازاتٌ لا تشكّل خطرًا على التّنفّس: النّيتروجين، والأكسجين، وبخار الماء (2NH4NO3 → 2N2 + O2 + 4H2O). لا يحدث التّحلّل التّامّ أبدًا، خاصّةً إذا كانت الظّروف غير متجانسة، وكمّيّات الموادّ كبيرة. إحدى الموادّ النّاتجة عن التّحلّل غير التّامّ لنيترات الأمونيوم هي أكسيد ثنائي النيتروجين المعروف بغاز الضّحك. مادة أخرى ناتجة عن التّحلّل هي ثاني أكسيدالنّيتروجين وهي مادّة سامّة، خاصّةً إذا تواجدت بتركيز عالٍ، لونها بنّيّ- أحمر، ومن المحتمل أنَّ انبعاث الدّخان الأحمر من موقع الانفجار يدلّ على وجود هذه المادّة.
أقرّت دول كثيرة قواعد مشدّدة لتخزين نيترات الأمونيوم بسبب المخاطر الّتي تترتّب عليه. تُحدّد هذه القواعد الكمّيّة القصوى من نيترات الأمونيوم الّتي يُسمح بتخزينها في مكان واحد، وأنواع الموادّ الّتي يًسمح بتخزينها بجانب مخازن نيترات الأمونيوم، والموادّ الّتي تتكوّن منها الحاويات الّتي تُعبَّأ وتُغلَّف فيها المادّة، وظروف التخزين، مثل التّهوئة والتّجفيف وأمان المخزن. العامل البشريّ هو المسبّب الرّئيسيّ لغالبيّة الكوارث الّتي نجمت عن نيترات الأمونيوم: الإهمال والاستهتار بالقواعد وجهل المخاطر. يبدو أنّ هذه هي العوامل الرّئيسيّة الّتي سبّبت انفجار بيروت أيضًا.
الترجمة للعربيّة: أ. خالد إبراهيم مصالحة
التدقيق اللغوي: أ. أديب أبو ريش
الإشراف العلمي والتحرير: رقيّة صبّاح أبو دعابس

