ניתוח תמונה ולמידת מכונה נכנסו לתחום הרפואה כבר לפני עשרות שנים. כלים כלים כאלה ועוד יישומי בינה מלאכותית יכולים לנתח כמויות גדולות של מידע ולסייע באבחון מחלות ואפילו במחקר – אבל יש להם גם מגבלות
הכתבה הוקלטה בידי הספרייה המרכזית לעיוורים ולבעלי לקויות ראייה
לרשימת כל הכתבות הקוליות באתר
השימוש בבינה מלאכותית בענפי הרפואה יצא לדרכו עוד כשתחום הבינה מלאכותית היה בחיתוליו, או לפחות בגיל ההתבגרות שלו. כבר בשנות ה-70 החלו חוקרים לשלב למידת מכונה – תת-תחום של תחום הבינה המלאכותית – בחקר בעיות רפואיות. עיבוד תמונה אוטומטי, השייך גם הוא לעולם הבינה המלאכותית, שימש באבחון באמצעות מחשבים מאז שנות ה-80. הטכנולוגיות האלו ויישומים נוספים של בינה מלאכותית, שהתפתחו והשתכללו במהלך העשורים שעברו, מוטמעים כיום בתחומים שונים של מדע הרפואה.

בינה מלאכותית היא כלי עזר יעיל במשימות רבות. רובוט ואדם תוקעים כף | ndrey_Popov, Shutterstock
מה מסתתר בתמונה?
אבחנות רפואיות רבות מסתמכות על פענוח של תמונות דימות רפואיות כמו רנטגן, CT ו-MRI. האבחנה מתבצעת על ידי רופאים שהתמחו גם בפענוח תמונות הדימות וגם בקביעת האבחנה הרפואית המסוימת. כלומר, כדי לפענח את תמונות הדימות ולקבוע לפיהן אבחנה רפואית דרושים איש או אשת מקצוע שעברו הכשרה ארוכה.
בשנים האחרונות, פיתוחים טכנולוגיים בתחום למידת המכונה החלו לשמש לניתוח תמונות דימות רפואיות – בהצלחה מרשימה. אבחון מוקדם של סרטן השד, למשל, מתבצע בעזרת צילום רנטגן של רקמת השד, הנקרא ממוגרפיה. אלגוריתמי בינה מלאכותית מצליחים לזהות אזורים חשודים בתמונות ממוגרפיה, וכך מסייעים לרופאים לבצע אבחנות מדויקות. בניסויים שבהם רופאים נעזרו בבינה מלאכותית כדי לאבחן סרטן ריאות, הם הגיעו לשיעור נמוך יותר של טעויות כאשר הבינה המלאכותית הצביעה על אזורים חשודים בתמונות הרדיולוגיות. גם בתחום הפתולוגיה, שבו רופאים בודקים דגימות מרקמות גופם של המטופלים, נמצא כי ניתוח ממוחשב יכול להביא תועלת רבה. בעבר התבוננו הרופאים בדגימות הרקמה מבעד למיקרוסקופ; כיום סורקים את הרקמות באמצעים דיגיטליים, ועיבוד ממוחשב של המידע שבתמונות יכול לסייע בתהליכי האבחון.
אבחון של מחלות מתבצע לא רק על פי תצלומים יחידים, אלא גם על סמך סרטונים: מחלות לב וכלי דם, למשל, מאובחנות בעזרת סרטוני אקו לב המתעדים את פעילות הלב. אלגוריתמי בינה מלאכותית המנתחים סרטוני אקו לב מסוגלים לזהות הבדלים עדינים בין מחזורי פעימות הלב, למדוד תפקודי לב ולהתריע על מקרים של אי-ספיקת לב.
בינות מלאכותיות יכולות לסייע גם בזמן אמת, במהלך הבדיקה עצמה. קולונוסקופיה, למשל, היא בדיקה פולשנית שבה מחדירים מצלמה זעירה למערכת העיכול התחתונה ובוחנים את דופנותיה כדי לאתר נגעים. במהלך הבדיקה עצמה אפשר לדגום את רקמות המעי באזורים חשודים, ולבדוק את הדגימות האלו בהמשך. מערכות סיוע ממוחשבות הפועלות במהלך הבדיקה מצליחות לזהות נגעים קטנים במיוחד, שלרופאים קשה להבחין בהם.
ג'פרי הינטון (Hinton), מאבות הבינה המלאכותית המודרנית, הקדים את זמנו באמון שנתן ביכולותיה. בכנס שנערך ב-2016 קרא הינטון להפסיק להכשיר רדיולוגים. ברור מאליו – כך טען – כי בינה מלאכותית תעקוף את הרדיולוגים ביכולותיה בתוך 5 עד 10 שנים. בהמשך תיקן הינטון את המלצתו: לא כדאי לוותר על הרדיולוגים, אלא להתקדם למצב שבו בינה מלאכותית קוראת את תמונות הדימות בעבור הרדיולוגים.
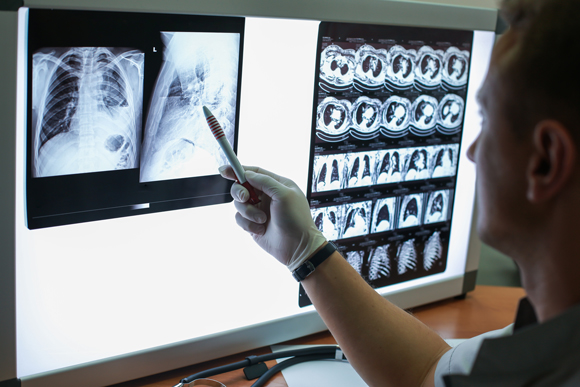
בינה מלאכותית יכולה לסייע לרופאים לאבחן מחלות על סמך תמונות דימות רפואיות. תמונת דימות של חולה ריאות | Egor_Kulinich, Shutterstock
לא כל כך מהר
כדי שמערכת מבוססת בינה מלאכותית תלמד לזהות כראוי אזורים בעלי עניין בתמונה רפואית, על המערכת ללמוד מתמונות רבות שעובדו, סומנו וסווגו בעבר על ידי בני אדם. תהליך הלימוד הזה מכונה ״אִימון״. אלגוריתמי בינה מלאכותית משתמשים במאגרים של תמונות מסומנות כדי לזהות בהן תבניות או כללים שניתן להכליל על תמונות חדשות.
מרכזים רפואיים שונים נבדלים זה מזה בציוד שבו הם משתמשים ליצירת תמונות הדימות, בתנאי הסביבה שבהם התמונה מצולמת, באופן שבו הרופאים מסמנים את התמונה לאחר הסיווג שלה וגם במאפייני האוכלוסייה המטופלת בהם. כל הבדל כזה יכול לפגוע ביכולת ההכללה של האלגוריתם. אלגוריתמים המתאמנים על תמונות שיוצרו בבית חולים אחד לא בהכרח ידעו להכליל כהלכה לתמונות שמיוצרות בבית חולים אחר. כאשר האלגוריתם מאומן בעבור אוכלוסיות מסוימות, הוא לא בהכרח ידע להכליל עבור אוכלוסיות אחרות המטופלות במוסד רפואי אחר. גם הסימונים הנהוגים במוסד הרפואי עלולים לפגוע בביצועי האלגוריתמים: לדוגמה, אלגוריתם מסוים למד לזהות תמונות של סרטן העור בעזרת סרגל שנכח בתמונות שבהן הגידול הוא ממאיר. למידה כזו מכונה למידה ״תוך כדי קיצורי דרך״ והיא הופכת את האלגוריתם לפחות יעיל כאשר הוא נתקל במידע בעל אופי מעט שונה. כדי להטמיע אמצעי בינה מלאכותית במרכז רפואי, יש צורך באימון מחדש או בהתאמת האימון של האלגוריתם למוסד מסוים זה. לשם כך על המוסד לספק אוסף גדול של נתונים מסווגים, המסומנים בצורה מדויקת ונקייה ככל האפשר מתוספות מיותרות.
נדגיש כי במשימות סיווג כאלו, למידת המכונה אינה יוצרת עבורנו ידע חדש: היא רק מסווגת בהתאם לדפוסים שזיהתה בדוגמאות שכבר הוכרעו על ידי רופאים. נוסף על כך, רופאים יכולים לנמק מדוע הם קיבלו החלטה מסוימת; בינה מלאכותית, לעומת זאת, פועלת במקרים רבים כמעין קופסה שחורה, וקשה להסביר מדוע האלגוריתמים הכריעו כפי שהכריעו.

בתהליך האימון, הבינה המלאכותית מתבססת על מאגר גדול של סיווגים קיימים כדי ללמוד להכליל מהם עבור מקרים חדשים. רובוט על ערמת ספרים קורא בספר | Vasilyev Alexandr, Shutterstock
עזר כנגדו
החוקר והנוירוכירורג אנטוניו די לבה (Di leva) שיער לפני שנים אחדות כי מכונות לא יחליפו רופאים, אולם רופאים הנעזרים בבינה מלאכותית יחליפו את הרופאים שנמנעים משימוש בה. גם אם לא נשאיר את כל משימת האבחון לבינה מלאכותית, ישנן תת-משימות שבהן היא משמשת ככלי עזר יעיל.
תהליכי העיבוד של תמונות דימות רפואיות כוללים כמה שלבים שונים של עיבוד תמונה, ברמות מורכבות שונות. עיבוד התמונה כולל גם ניקוי של המידע שבה מרעשי רקע בלתי נמנעים. על ידי ניקוי רעש הרקע, אלגוריתמי למידת מכונה יכולים לשפר ולהגדיל את הרזולוציה של תמונות דימות רפואיות. כאשר התמונה מוכנה לפענוח, אחת המשימות שאפשר לבצע היא זיהוי אזורי העניין שבה. המשימה של חלוקת התמונה לאזורי עניין מכונה סגמנטציה (segmentation). מיפוי של פעולות הלב, למשל, דורש תיחום של חלקי הלב, כגון החדרים והעליות, כדי להעריך את אופי הפעילות שלהם. סגמנטציה באמצעות בינה מלאכותית מאפשרת תיחום לא רק ברמה האנטומית – של איברים, כמו חדרי הלב – אלא גם ברמת הרקמות הנראות בתמונת מיקרוסקופ. יישומי בינה מלאכותית מסוגלים, למשל, לנתח תמונת מיקרוסקופ ולתחום בתוכה אזורים של רקמות סרטניות.
אחרי משימות התיחום וזיהוי הנגעים, מגיעות משימות הסיווג (classification). האלגוריתמים מאומנים לסווג את הנגע ולקבוע אם הוא שפיר או סרטני, ואם הוא סרטני, מהו סוג הסרטן. כיום כבר ישנם אלגוריתמים שאומנו לנתח תמונות של נגעים בעור ולסווג אותם לסוגים שונים של סרטן עור, ברמות סיכון שונות.
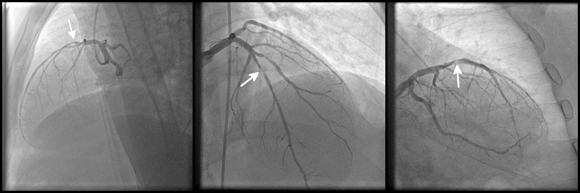
כל סימן נוסף בתמונה מלבד הדגימה או הצילום הרפואי עצמו - עלול לגרור אימון שגוי של האלגוריתם. תמונת דימות של מחלת לב כלילית | kalewa, Shutterstock
לחזות את העתיד
משימה מורכבת וחשובה במיוחד היא משימת החיזוי – למשל, מהי רמת הסיכון של המטופל לאור האבחנה, או מה קצב התקדמות המחלה. חוקרים מנסים לפתח בינות מלאכותיות שיוכלו לבצע חיזויים כאלה. לדוגמה, במחקר מסוים הצליחו חוקרים לאמן בינה מלאכותית לנתח תמונות CT ולקבוע לפיהן מראש מי מהנבדקים נמצא בסיכון לפתח סרטן ריאות, וזאת בין שנה ל-6 שנים לפני הופעת המחלה. החוקרים מצאו שהאלגוריתם מזהה מאפיינים שידועים כסימנים מוקדמים לסרטן ריאות. גם בסרטן השד ישנם סימנים מקדימים שיכולים לעזור לחזות סיכון גבוה להתפתחות סרטן השד בעתיד.
אך מידע רפואי אינו מגיע, כמובן, רק בצורת תמונות דימות, אלא גם כמדדים של בדיקות דם, כמו רמת הסוכר ומספר תאי הדם האדומים; כמידע גנטי שנמצא בבדיקות DNA; כסוגים וכמויות של חיידקים שונים במעיים שלנו, שנמצאו בעזרת בדיקות מיקרוביום, ועוד. במחקר של ארגון הבריאות הישראלי "כללית" פיתחו החוקרים מודל חיזוי המתריע על מטופלים הנמצאים בסיכון מוגבר ללקות בתוך כמה שנים באי-ספיקת כליות כרונית. מחקרים מפתחים תחזיות עבור מחלות נוספות, כמו מחלות לב וכלי דם וסוכרת.
לכלים אלה יש חשיבות רבה מאוד: הם עשויים לספק לנו התראה מקדימה על מחלות שמטופל מסוים עלול לסבול מהן ולאפשר היערכות, מניעה וטיפול טובים ככל האפשר. עם זאת, חשוב לשים לב שחיזוי מראש רלוונטי בעיקר למחלות המתפתחות באיטיות ובהדרגה. מגבלה זו מצמצמת את טווח המחלות שכלים אלה רלוונטיים לגביהן.

מכונת משחקים אוטומטית, המכילה מגוון "תחזיות" לעתיד, שולפת אחת מהן בצורה אקראית כאשר מפעילים אותה, ואילו מודל חיזוי מוצלח מספק לנו חיזוי טוב בהרבה מניחוש אקראי. מכונת זולטר מגיד העתידות | Darryl Brooks, Shutterstock
פאזל מורכב
ככל שהטכנולוגיה מתפתחת, אנו מסוגלים למדוד גורמים רבים יותר בגוף המטופלים במידה רבה יותר של דיוק. לבני אדם קשה לתפוס קשר בין משתנים מרובים; למכונה, לעומת זאת, פחות אכפת כמה משתנים שונים היא תקבל. מחקרים שונים נעזרים ביכולות ממוחשבות כדי לנתח כמויות גדולות של מידע מגוון ולזהות קשרים מורכבים המעידים על מצבי בריאות שונים. כך, למשל, מחקרים שונים מצאו קשר בין מאפיינים של רשתית העין, שאפשר לזהות אותם בתמונות, ובין מחלת כליות, מחלות לב ומחלת אלצהיימר.
אך חשוב להבין כי מציאת קשר מורכב עדיין אינה מספקת לנו הבנה אמיתית של המערכת הביולוגית, ועוד פחות מזה – פתרון או ריפוי למחלה. שימוש בלמידת מכונה מאפשר לנו להביא בחשבון משתנים מרובים ולנתח כמויות גדולות של מידע, אבל כדי לפתח שיטת ריפוי, צריך להבין מה מקור הבעיה.
מה מקור המידע?
כדי שמודל בינה מלאכותית ילמד לסווג מידע רפואי ולספק לפיו חיזוי אמין של התפתחות מחלות אצל המטופל, עליו לקבל מידע מדויק ובלתי מוטה. הטיות, כאמור, נמצאות בכל מקום, החל מהציוד שבו משתמשים כדי לקחת את הדגימה, דרך האדם שמבצע את העיבוד של הדגימה ועד האוכלוסייה שממנה נלקחות הדגימות. הטיה משמעותית המאפיינת מידע רפואי שמקורו בבתי חולים ובמרכזים רפואיים היא שמי שמגיע לרופא, כנראה כבר איננו בקו הבריאות. רובנו איננו הולכים סתם כך לבדיקות רפואיות, בייחוד למחלות נדירות. ישנן מחלות שהמודעות אליהן גבוהה יותר, כמו סרטן השד, שזוכה לקמפיינים שנתיים הקוראים לציבור להיבדק. אבל גם במקרה החריג הזה, ברור שאנשים עם גישה פחות נוחה לבדיקות יגיעו פחות להיבדק. זה עלול ליצור חוסר בדגימה של אוכלוסיות מעוטות יכולת. המחסור במידע מאוזן מחריף ככל שמדובר במחלות נדירות יותר. כדי להשלים את החסר, ישנם פרויקטים שונים האוגרים לאורך זמן מידע רפואי של קבוצות מתנדבים רחבות ואקראיות ככל האפשר. המאגר הבריטי UK Biobank מכיל מידע מחצי מיליון מתנדבים החל מ-2006. בישראל נאספים נתונים רפואיים במאגרים שונים, כמו המאגר הלאומי פסיפס ופרויקט 10K.

אוסף של מדדים שונים מאנשים רבים מאפשר חיפוש אחר קשרים מורכבים בתופעות בריאותיות. איור להמחשת שילוב טכנולוגיה וניתוח נתונים לטובת הרפואה | ArtemisDiana, Shutterstock
פתיתי שלג ייחודיים
איסוף וניתוח נתונים מהאוכלוסייה הכללית אינם מספיקים כדי לתת מענה לחולים פרטניים. לכל אחד מאיתנו יש מדדים אופייניים הנמצאים בטווח הנורמלי בעבורנו כשאנחנו בריאים. סטייה ממצב נורמלי זה יכולה להעיד על מחלה או מצב רפואי לא-תקין. השונוּת באוכלוסייה, כלומר ההבדל במדדים בין אדם אחד לאחר, יכולה להיות גדולה מאוד. בבדיקת דם של מטופל יכול להופיע ערך חריג ביחס לאוכלוסייה, אבל לא חריג ביחס למצב הבריא של המטופל עצמו; ולהפך, ייתכן שיופיע בה ערך שנמצא בטווח הנורמלי ביחס לממוצע של כל האוכלוסייה, אבל הוא חריג מאוד בעבור המטופל. כלומר, השונות הגבוהה באוכלוסייה עלולה למסך סימנים לסטיות במצב הבריאותי של מטופל או מטופלת מסוימים.
כדי לזהות שינוי חריג במדדים של מטופל, צריך לעקוב אחריו לאורך זמן ולזהות סטייה מן המדדים שלו-עצמו. איסוף מידע אישי לאורך זמן הוא אתגר בפני עצמו, שיכול לקבל מענה במדינות כמו ישראל, שבהן כמעט כל אזרח שייך לקופת חולים מיום היוולדו והרשומות הרפואיות שלו נאגרות לאורך זמן; אבל ברוב המדינות זה איננו המצב. טכנולוגיה לבישה כמו שעונים חכמים מאפשרת לאתר סטיות במצב הרפואי של מי שעונד אותם; שעונים חכמים מסחריים מאפשרים מעקב אחרי מדדים שונים בעזרת מד דופק, מד סטורציה (רמת חמצן בדם) ועוד, וכבר התריעו בעבר לעונדים אותם על מדדים חריגים, וכך אפשרו אבחון רפואי מציל חיים.

השונות הגדולה באוכלוסייה אינה מעידה על המאפיינים של מטופל מסוים. זרקור על מספר אנשים מתוך המון | alphaspirit.it, Shutterstock
אדם מול מכונה
נוסף על אבחון של מצבים רפואיים, בינה מלאכותית משמשת בתחומים רבים שבהם מדע הרפואה משיק לטכנולוגיה. כמה מתחומים אלה הם פיתוח ציוד רפואי, חיפוש ופיתוח תרופות, סוגיות תיאורטיות כמו חיזוי המבנה של חלבונים ועוד.
לצד היתרונות של למידת מכונה, חשוב לזכור גם את המגבלות שלה. אם תהליך הלמידה של הבינה המלאכותית משתמש בידע רפואי קיים – למשל, אם ידוע שמבנה מסוים של רקמה מעיד על נגע סרטני – הסיווג שמבצעת המכונה אומנם חוסך זמן יקר של אנשי סגל רפואי, אבל אינו מייצר בעבורנו ידע רפואי חדש. יתרה מזו: ההטמעה של כלי בינה מלאכותית במערך הרפואי אינה עניין פשוט, וגם היא דורשת השקעה של מאמץ ומשאבים. ולבסוף, כפי שראינו, אומנם למידת מכונה מאפשרת לנו לנתח כמויות גדולות של מידע, לעקוב אחר משתנים רבים, לזהות קשרים מורכבים ביניהם ולבצע חיזוי למצבם הרפואי של המטופלים בעתיד, אבל היא אינה מספקת הסבר למנגנון שעומד מאחורי הקשרים האלו. כדי למצוא מרפא לבעיה הרפואית עצמה, צריך להבין את המנגנון הגורם לה. בינה מלאכותית היא כלי מצוין לשיפור יכולת החיזוי, האבחון והמחקר שלנו, אך היא אינה תחליף למחקר ולמחשבה של בני אדם.
